近日,中南大学湘雅药学院周文虎教授团队在生物材料领域国际顶尖期刊《Biomaterials》上发表了题为“Multifunctional selenium nanoplatforms for synergistic ferroptosis inhibition and immune microenvironment remodeling in oral mucositis”的最新研究成果。该研究创新性地揭示了铁死亡(Ferroptosis)是驱动口腔黏膜炎(OM)进展的核心病理机制,并开发了一种集“强效黏附、精准抗氧、免疫调控”于一体的聚血清素功能化硒纳米治疗平台(PST-SeNPs),为突破口腔黏膜修复瓶颈提供了新策略。
【研究背景:临床痛点与机制瓶颈】
口腔黏膜炎(OM)是放射治疗、化学治疗及免疫功能低下人群常见的致残性并发症,临床表现为剧烈疼痛、多发性溃疡及上皮屏障受损。目前临床治疗多局限于镇痛、抗菌等对症处理,疗效欠佳。究其原因,OM的病理微环境极为复杂,涉及上皮损伤(“种子”)与局部免疫失衡(“土壤”)的恶性协同,单一靶点的干预策略难以阻断病情迁延,严重影响患者的生活质量及原发病的治疗进程。
【核心发现:锁定铁死亡驱动的新机制】
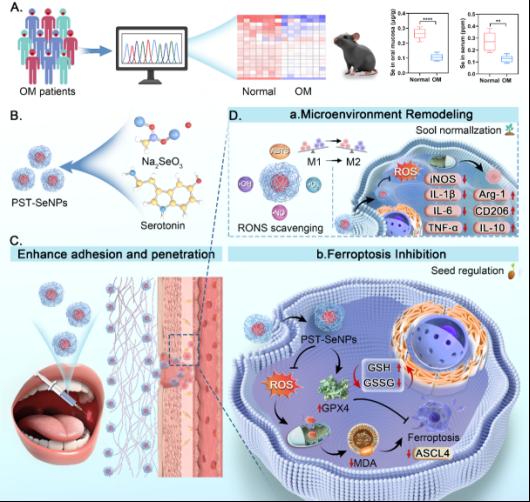
针对这一困境,研究团队通过临床样本分析与转录组学研究,首次证实了硒(Se)代谢紊乱与谷胱甘肽过氧化物酶4(GPX4)表达下调是驱动OM进展的关键诱因。研究指出,硒代谢失衡会导致脂质过氧化物在黏膜组织中过度累积,进而触发上皮细胞铁死亡。这一发现精准定位了OM发病过程中的分子串扰机制,确立了以抑制铁死亡为核心,同步缓解氧化损伤、抑制炎症、保护上皮的多效合一治疗新方向。
【技术突破:构建“种子-土壤”整合治疗平台】
基于上述机制发现,团队理性设计并构建了PST-SeNPs多功能纳米治疗平台。该平台具有三大核心技术优势:
Ø 卓越的黏膜滞留与渗透能力:利用聚血清素(PST)极强的生物黏附特性,有效解决了传统药物易被唾液冲刷、在口腔病灶停留时间短的难题,实现了药物在溃疡区域的深部渗透与长效释放。
Ø “种子-土壤”双重修复策略:该纳米平台通过高效外源性补硒恢复GPX4活性,直接保护黏膜上皮(“种子”)免于铁死亡损伤;同时诱导巨噬细胞向抗炎M2型极化,重塑局部免疫微环境(“土壤”)。
Ø 多机制协同增效:实验结果显示,PST-SeNPs在清除活性氧(ROS)、抑制炎症风暴及促进微血管修复方面显著优于常规硒制剂,成功逆转了“氧化应激–铁死亡–炎症放大”的病理恶性循环。
【评价与展望】
在体内外模型实验中,仅需隔日给药即可显著加速口腔溃疡愈合,并表现出优异的生物安全性。该研究不仅深化了对口腔黏膜类疾病分子机制的科学认知,更为复杂炎症性疾病中“氧化还原平衡-细胞死亡调控-免疫稳态”的整合型纳米药物开发提供了具有临床转化潜力的通用型平台。
【作者与资助信息】
中南大学湘雅药学院欧阳琴博士为该论文第一作者,周文虎教授为唯一通讯作者。该研究工作得到了国家自然科学基金等项目的资助。
原文链接:https://doi.org/10.1016/j.biomaterials.2026.124147
(一审:周文虎,二审:陈传品,三审:曹东升)
